Раздельное растворение марганца и его окислов
Раздельное растворение марганца и его окислов
Может у кого есть мысли, как это сделать? Задача состоит в том, что есть порошок, содержащий марганец и смесь его окислов. Нужно перевести в р-р или марганец, или его окислы для дальнейшего анализа. Или как раздельно определить марганец.
Re: Раздельное растворение марганца и его окислов
Как мне кажется,сначало погреть смесь что бы не осталось вероятно имеющихся гидроксидов. Потом в раствор нашатыря,хлорид аммония. По идее металл растворится,оксиды нет. Но не уверен
Это может быть не просто,но это может быть!
Истина может и на вашей стороне,но не забывайте и о другой
Истина может и на вашей стороне,но не забывайте и о другой
- Droog_Andrey
- Сообщения: 2670
- Зарегистрирован: Сб сен 29, 2007 8:29 pm
- Контактная информация:
Re: Раздельное растворение марганца и его окислов
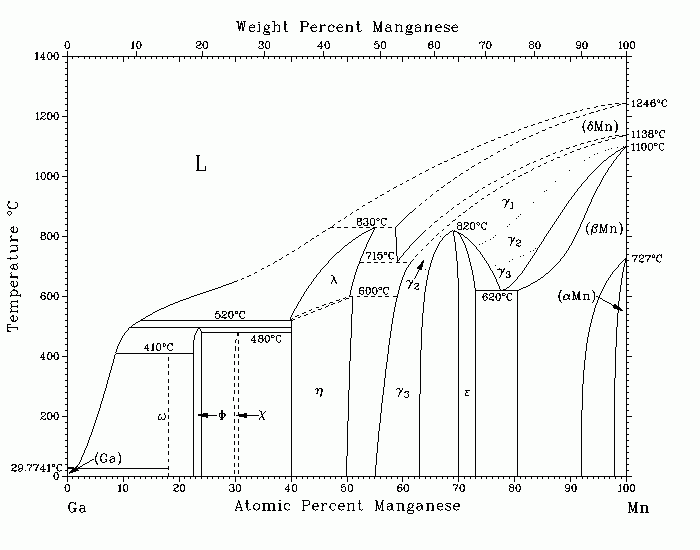
Жидкий галлий растворяет несколько процентов марганца при небольшом нагревании:

2^74207281-1 is prime!
Re: Раздельное растворение марганца и его окислов
Это был тест на вменяемость?
dmr-a тупо отсеиваем(не забыть ему сказать, что любим )
)
А так задача любопытная.
dmr-a тупо отсеиваем(не забыть ему сказать, что любим
А так задача любопытная.
Бог на стороне не больших батальонов, а тех, кто лучше стреляет (приписывается Вольтеру)
- Droog_Andrey
- Сообщения: 2670
- Зарегистрирован: Сб сен 29, 2007 8:29 pm
- Контактная информация:
Re: Раздельное растворение марганца и его окислов
Ну а вдруг у чувака совершено случайно стоит рояль в кустах ведро жидкого галлия? 
2^74207281-1 is prime!
Re: Раздельное растворение марганца и его окислов
А чего так тупо то,амик?
Выж химик а не с .. гранта.
Ну а по правде скажите,не ответь я в эту тему,спустились бы в с вершины своего высокомерия,и ответили бы в тему?((
Ну а по теме,если мне все же кажется монооксиду марганцу не хватит ph раствориться в нашатыре,и диоксиду
Выж химик а не с .. гранта.
Ну а по правде скажите,не ответь я в эту тему,спустились бы в с вершины своего высокомерия,и ответили бы в тему?((
Ну а по теме,если мне все же кажется монооксиду марганцу не хватит ph раствориться в нашатыре,и диоксиду
Это может быть не просто,но это может быть!
Истина может и на вашей стороне,но не забывайте и о другой
Истина может и на вашей стороне,но не забывайте и о другой
Re: Раздельное растворение марганца и его окислов
После того, как вы спрашиваете вчера на химике, что получится при смешивании пищевой соды NaHCO3 и дигидрофосфата натрия NaH2PO4, вы не можете претендовать... или можете и имеете право.
При том, что люблю я вас по-прежнему
При том, что люблю я вас по-прежнему
Бог на стороне не больших батальонов, а тех, кто лучше стреляет (приписывается Вольтеру)
Re: Раздельное растворение марганца и его окислов
Грубо - рентгенофазовый.smihailov писал(а):Может у кого есть мысли, как это сделать? Задача состоит в том, что есть порошок, содержащий марганец и смесь его окислов. Нужно перевести в р-р или марганец, или его окислы для дальнейшего анализа. Или как раздельно определить марганец.
Бог на стороне не больших батальонов, а тех, кто лучше стреляет (приписывается Вольтеру)
Re: Раздельное растворение марганца и его окислов
Дык беда в том, что марганец практически в любой среде начнет растворяться с выделением "активного водорода", который начнёт восстанавливать высшие окислы марганца. Хотел было вначале предложить волюмометрию, основанную на выделении водорода, но по здравому размышлению, отказался.dmr писал(а):Ну а по теме,если мне все же кажется монооксиду марганцу не хватит ph раствориться в нашатыре,и диоксиду
Бог на стороне не больших батальонов, а тех, кто лучше стреляет (приписывается Вольтеру)
Re: Раздельное растворение марганца и его окислов
Один из способов получения марганца.
6. Электролиз с ртутным катодом. Относительно чистый марганец может быть получен при электролизе водного раствора марганцевой соли с использованием ртутного катода. Марганцевая амальгама, образующаяся при этом, фильтруется, а ртуть дистиллируется в вакууме. Этот метод был впервые использован Муассаном, а позже Гэнтцом. К недостаткам метода следует отнести то, что полученный марганец, хотя и достаточно чист, но представляет собой тонкий порошок, в связи с чем он легко окисляется, и часто пирофорен. Гэнтц обнаружил, что реакционная способность порошкового марганца уменьшается по мере повышения температуры, при которой происходит дистилляция ртути.
6. Электролиз с ртутным катодом. Относительно чистый марганец может быть получен при электролизе водного раствора марганцевой соли с использованием ртутного катода. Марганцевая амальгама, образующаяся при этом, фильтруется, а ртуть дистиллируется в вакууме. Этот метод был впервые использован Муассаном, а позже Гэнтцом. К недостаткам метода следует отнести то, что полученный марганец, хотя и достаточно чист, но представляет собой тонкий порошок, в связи с чем он легко окисляется, и часто пирофорен. Гэнтц обнаружил, что реакционная способность порошкового марганца уменьшается по мере повышения температуры, при которой происходит дистилляция ртути.
Сократ мне друг, но истина дороже.
Re: Раздельное растворение марганца и его окислов
Любовь и вечный ваш оргазм,не спутайте в одном месте...amik писал(а):После того, как вы спрашиваете вчера на химике, что получится при смешивании пищевой соды NaHCO3 и дигидрофосфата натрия NaH2PO4, вы не можете претендовать... или можете и имеете право.
При том, что люблю я вас по-прежнему
"А ты не путай свою личную шерсть с государственной"
Кавказская пленница
Там суть вопроса о том как,а ни что?
Это может быть не просто,но это может быть!
Истина может и на вашей стороне,но не забывайте и о другой
Истина может и на вашей стороне,но не забывайте и о другой
Re: Раздельное растворение марганца и его окислов
А нельзя ли отдельно растворить имеено марганец в растворах солей меди? Оксид то на это пожалуй не отреагирует??? Хотя и загрязнится медью
Это может быть не просто,но это может быть!
Истина может и на вашей стороне,но не забывайте и о другой
Истина может и на вашей стороне,но не забывайте и о другой
Re: Раздельное растворение марганца и его окислов
[quote="amik Грубо - рентгенофазовый.[/quote]
Действительно грубо, объект - шлак с металлом, погрешность большая, но на безрыбье ... . Лучше бы на волновом РФА с гониометром попробовать, но где его взять?
Действительно грубо, объект - шлак с металлом, погрешность большая, но на безрыбье ... . Лучше бы на волновом РФА с гониометром попробовать, но где его взять?
Re: Раздельное растворение марганца и его окислов
2 stallker
Мы перекрестились, когда избавились от ртути.
Мы перекрестились, когда избавились от ртути.
Re: Раздельное растворение марганца и его окислов
Если задача аналитическая, то иодометрически никак?
"Я не видел людей страшней, чем толпа цвета хаки"
Re: Раздельное растворение марганца и его окислов
А почему не гравиметрией?
Классика же...
Взвесить -> растворить -> осадить -> прокалить -> взвесить. И посчитать.
Классика же...
Взвесить -> растворить -> осадить -> прокалить -> взвесить. И посчитать.
Re: Раздельное растворение марганца и его окислов
Может вы чего не поняли? С анализом нет вопросов. Вопрос в избирательном растворении!
Re: Раздельное растворение марганца и его окислов
Отдельно растаорять придется все же металл,или за счет его восстановительной способности с солями менее активных металлов,той же меди,или 10-15 кратным избытком легкоплавких сплавов (Pb,Zn,Sn...)но при температурах за 500
Это может быть не просто,но это может быть!
Истина может и на вашей стороне,но не забывайте и о другой
Истина может и на вашей стороне,но не забывайте и о другой
Re: Раздельное растворение марганца и его окислов
А Александр с Вами с пользой поработал. А окислы при этом не восстановятся?dmr писал(а):Отдельно растаорять придется все же металл, 10-15 кратным избытком легкоплавких сплавов (Pb,Zn,Sn...)но при температурах за 500
Re: Раздельное растворение марганца и его окислов
Проблема, как понимаю, ещё и в том, что шлак представляет собой тесную спеченную смесь фаз, причём часть металла может быть закапсулирована окислами. Т.е. даже при кислотной обработке нет уверенности, что весь марганец прореагирует?
Бог на стороне не больших батальонов, а тех, кто лучше стреляет (приписывается Вольтеру)
Кто сейчас на конференции
Сейчас этот форум просматривают: нет зарегистрированных пользователей и 25 гостей