Понятное дело, что понятия приближённые. Я о том, что можно эту степень приближённости представлять и пользоваться этими представлениями. А то есть любители отсутствие понимания прикрывать убеждениями о бесполезности понятия (см. тему о степени окисления -5, например)
Спор о фазах, природе химической связи, валентности и степени окисления
- Droog_Andrey
- Сообщения: 2699
- Зарегистрирован: Сб сен 29, 2007 8:29 pm
- Контактная информация:
Re: Спор о фазах, природе химической связи, валентности и степени окисления
И CO+, и N2+ оба 2Σ, но в N2+ "подтягивания" не происходит  В то же самое время при ионизации BF "подтягивание" сильнее, чем в CO, но при этом в BF связь заметно длиннее, чем в BF2+, где она вроде как двойная по всем канонам
В то же самое время при ионизации BF "подтягивание" сильнее, чем в CO, но при этом в BF связь заметно длиннее, чем в BF2+, где она вроде как двойная по всем канонам 
Понятное дело, что понятия приближённые. Я о том, что можно эту степень приближённости представлять и пользоваться этими представлениями. А то есть любители отсутствие понимания прикрывать убеждениями о бесполезности понятия (см. тему о степени окисления -5, например)
Понятное дело, что понятия приближённые. Я о том, что можно эту степень приближённости представлять и пользоваться этими представлениями. А то есть любители отсутствие понимания прикрывать убеждениями о бесполезности понятия (см. тему о степени окисления -5, например)
2^74207281-1 is prime!
Re: Спор о фазах, природе химической связи, валентности и степени окисления
В случае с N2 это другая "Σ"Droog_Andrey писал(а): ↑Ср май 09, 2018 12:39 pmИ CO+, и N2+ оба 2Σ, но в N2+ "подтягивания" не происходитВ то же самое время при ионизации BF "подтягивание" сильнее, чем в CO, но при этом в BF связь заметно длиннее, чем в BF2+, где она вроде как двойная по всем канонам

В молекуле N2 ионизируется связывающее молекулярное состояние сигма-g, образующееся при комбинации двух атомных состояний pz.
Поэтому тут снижается электронная плотность не на атомно-локализованном, а наоборот, на связывающем состоянии, и связь ослабляется.
Кстати, следующий первый потенциал ионизации приводит к молекулярному терму 2П -- тоже ионизируется связывающее состояние, тоже ослабляется связь. А вот следующий ППИ приводит к иону с молекулярным термом 2Σu (ионизируется то же разрыхляющее 2s-состояние, что и в молекуле CO), и вот тут-то связь укорачивается.
Данная тема тоже со всей очевидностью показывает вред от непонимания приближений и ограничений, а также от российской школьной программы, в которой многие понятия (в т.ч. валентность) интерпретируются на доквантовом уровне понимания ("чёрточки"). Хотя химия по самой своей природе (по объекту исследования) -- чисто квантовая отрасль.Droog_Andrey писал(а): ↑Ср май 09, 2018 12:39 pmПонятное дело, что понятия приближённые. Я о том, что можно эту степень приближённости представлять и пользоваться этими представлениями. А то есть любители отсутствие понимания прикрывать убеждениями о бесполезности понятия (см. тему о степени окисления -5, например)
When you open your heart to patriotism, there is no room for prejudice.
- Droog_Andrey
- Сообщения: 2699
- Зарегистрирован: Сб сен 29, 2007 8:29 pm
- Контактная информация:
Re: Спор о фазах, природе химической связи, валентности и степени окисления
Да та же самая там сигма. И атомной локализованности там нет, есть некоторая асимметричность орбитали (из-за неё и минус на углероде). При отрыве электрона от цианид-аниона связь тоже, кстати, укорачивается, но не так сильно, как в CO. Приписывание сигмы сугубо к 2s либо сугубо к 2pz - чистейшей воды произволchaus писал(а): ↑Ср май 09, 2018 5:01 pmВ случае с N2 это другая "Σ"
В молекуле N2 ионизируется связывающее молекулярное состояние сигма-g, образующееся при комбинации двух атомных состояний pz.
Поэтому тут снижается электронная плотность не на атомно-локализованном, а наоборот, на связывающем состоянии, и связь ослабляется.
2^74207281-1 is prime!
Re: Спор о фазах, природе химической связи, валентности и степени окисления
Простите, но это совершенно разные сигмы!Droog_Andrey писал(а): ↑Чт май 10, 2018 12:49 pmДа та же самая там сигма. И атомной локализованности там нет, есть некоторая асимметричность орбитали (из-за неё и минус на углероде). При отрыве электрона от цианид-аниона связь тоже, кстати, укорачивается, но не так сильно, как в CO. Приписывание сигмы сугубо к 2s либо сугубо к 2pz - чистейшей воды произволchaus писал(а): ↑Ср май 09, 2018 5:01 pmВ случае с N2 это другая "Σ"
В молекуле N2 ионизируется связывающее молекулярное состояние сигма-g, образующееся при комбинации двух атомных состояний pz.
Поэтому тут снижается электронная плотность не на атомно-локализованном, а наоборот, на связывающем состоянии, и связь ослабляется.
Σg, которая высшая по энергии в молекуле N2 -- связывающая, в ней действительно нет атомной локализации и она получается именно при перекрывании двух pz.
Σ, высшая по энергии в молекуле CO -- разрыхляющая, локализованная на углероде и происходящая, в сущности, из практически чистой C2s.
В цианиде то же самое.
Ну, высоконько лежит C2s по сравнению с N2p и O2p, не говоря уже про N2s и O2s. Поэтому и торчит так некрасиво в спектрах CO и CN(-).
См.: Roger L. DeKock, Harry B. Gray. Chemical Structure And Bonding. 1989. Схема на стр. 240 и табл. на стр. 241.
Приписывание молекулярных состояний тем или иным атомным -- не чистый произвол, а расчёт расщепления с учётом интегралов перекрывания и, самое главное, прямых измерений электронных спектров. Для сильно смешанных связывающих состояний разложение по атомным действительно содержит большую долю формализма, но для разрыхляющих, локализованных на том или ином атоме, сходство с соответствующими атомными состояниями -- факт.
When you open your heart to patriotism, there is no room for prejudice.
- Avak_Avakyan
- Сообщения: 95
- Зарегистрирован: Пн июн 15, 2015 10:08 pm
Re: Спор о фазах, природе химической связи, валентности и степени окисления
Ох…  Итак, давайте откроем УЧЕБНИКИ…
Итак, давайте откроем УЧЕБНИКИ…  Для начала парочка цитат из Химической энциклопедии: «КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ, то же, что координационные соединения.». Далее: «КООРДИНАЦИОННЫЕ СОЕДИНЕНИЯ (комплексные соед.)». То есть не надо делить, что «комплекс» — это, якобы, обязательно жёсткая координация вокруг некоего атома. Далее. Откроем «Курс “Химия” для студентов инженерно−технических специальностей. Лекционный курс. Тема 3. Растворы и дисперсные системы. Межмолекулярное взаимодействие, комплексные соединения.»: Цитата: «Комплексные соединения — это особая группа молекулярных соединений, состав которых нельзя объяснить с позиций классической теории валентности. Оказалось, что наряду с соединениями первого порядка BF3, H2O, CO2, где элемент проявляет максимальную обычную валентность (валентнонасыщенные соединения), существуют соединения высшего порядка (при взаимодействии соединений первого порядка друг с другом). Пример: BF3+HF=H[BF4]. Альфред Вернер в конце 19 вèка ввёл в химию понятие о соединениях высшего порядка… Вернер высказал предположение, что любой элемент после насыщения его обычных валентностей способен проявлять дополнительную координационную валентность. И именно за счёт этой валентности образуются соединения высшего порядка.». Есть и УЧЕБНИК, более точно расставляющий точки над “ё”
Для начала парочка цитат из Химической энциклопедии: «КОМПЛЕКСНЫЕ СОЕДИНЕНИЯ, то же, что координационные соединения.». Далее: «КООРДИНАЦИОННЫЕ СОЕДИНЕНИЯ (комплексные соед.)». То есть не надо делить, что «комплекс» — это, якобы, обязательно жёсткая координация вокруг некоего атома. Далее. Откроем «Курс “Химия” для студентов инженерно−технических специальностей. Лекционный курс. Тема 3. Растворы и дисперсные системы. Межмолекулярное взаимодействие, комплексные соединения.»: Цитата: «Комплексные соединения — это особая группа молекулярных соединений, состав которых нельзя объяснить с позиций классической теории валентности. Оказалось, что наряду с соединениями первого порядка BF3, H2O, CO2, где элемент проявляет максимальную обычную валентность (валентнонасыщенные соединения), существуют соединения высшего порядка (при взаимодействии соединений первого порядка друг с другом). Пример: BF3+HF=H[BF4]. Альфред Вернер в конце 19 вèка ввёл в химию понятие о соединениях высшего порядка… Вернер высказал предположение, что любой элемент после насыщения его обычных валентностей способен проявлять дополнительную координационную валентность. И именно за счёт этой валентности образуются соединения высшего порядка.». Есть и УЧЕБНИК, более точно расставляющий точки над “ё”  [А.Н. Морозов. Теория строения координационных соединений. Курс лекций для студентов химфака ЮФУ (РГУ)]: Цитирую: «ИСТОРИЯ КООРДИНАЦИОННОЙ ХИМИИ
[А.Н. Морозов. Теория строения координационных соединений. Курс лекций для студентов химфака ЮФУ (РГУ)]: Цитирую: «ИСТОРИЯ КООРДИНАЦИОННОЙ ХИМИИ
Некоторые определения координационного соединения
1. Первая попытка классификации, включающей в себя комплексные соединения, заключалась в рассмотрении их с позиций соблюдения или несоблюдения правил формальной валентности. При этом соединения подразделялись на два класса — простые (атомные) и комплексные (молекулярные).
Вследствие того, что в комплексном соединении АВ исходные атомные соединения А и В сохраняют свою индивидуальность, считалось, что комплексы не могут переходить без разложения в парообразное состояние. Однако данная классификация перестала быть актуальной после 1893 гòда, когда был получен ряд соединений, не разлагавшихся при переходе в парообразное состояние. Тезис о сохранении индивидуальности исходных компонентов в комплексе был необходим для того, чтобы к координационным не относились такие соединения, как, например, серная кислота, получаемая по реакции соединения двух атомных соединений SO3 и Н2О.». Ниже приводится таблица, которую я в виде картинки приложил сюда: Заметьте, что именно позиции из этой таблицы я здесь (ужè столько времени) объясняю. Далее в этом учебнике приводятся определения, которые давались позже, и их заслуженная критика. Мне нравится определение, которое в 1933 годỳ (через 40 лет ПОСЛЕ Вернера) дал Ф. Файгль: «координационное соединение — это соединение, строение которого не может быть объяснено нормальным числом валентных связей».
Следует подчеркнуть важный факт: ИОННЫЕ и КОВАЛЕНТНЫЕ соединения де−факто имеют одну природу и различаются лишь СТЕПЕНЬЮ ионности, которая, как правило, тем выше — чем больше разница между соединёнными атомами; например, LiF ионнее BeO, который ионнее BN. Кроме того, «Известно, что ионная и ковалентная связи, а также ковалентная и металлическая не имеют резкого разграничения и может наблюдаться переход от одного вида связи к другому.» [И.Я. Клинов. Коррозия химической аппаратуры и коррозионностойкие материалы. Машиностроение. Москва. 1967].
Ещё цитата: «Комплексным соединением называется соединение высшего порядка, образующееся из соединений первого порядка без образования новых электронных пар, а за счёт проявления хотя бы одной координативной связи.» [Я.И. Михайленко. Курс общей и неорганической химии. Высшая школа. Москва 1966. Стр. 119]. То есть опять же: есть МОЛЕКУЛЫ — это соединения первого порядка, то есть ВАЛЕНТНЫЕ соединения, склеенные только валентными электронами; а есть ассоциаты — продукты налипания одной молекулы на другую, и эта межмолекулярная связь «ненастоящая», НЕвалентная.
Вас возмущает «рисование чёрточек» применительно к ионной связи, но почему тогда Вас не возмущают эти чёрточки в CIF−файлах структур алюминатов; ведь кристаллическая решётка сапфира считается ионной? А теперь факт: в структурных формулах металлохелатов ПРИНЯТО рисовать ИОННЫЕ связи чёрточками, а вот комплексные связи в них рисуют СТРЕЛКАМИ! Пример из всё того же учебника:

Надеюсь, Вы не будете доказывать, что связь меди в её енолятах неионная.
Из Химической энциклопедии: «КООРДИНАЦИOННАЯ СВЯЗЬ, хим. связь в комплексных соединениях, в к−рых один или неск. атомов образуют большее число связей, чем допускает высшая формальная валентность этих атомов.» — опять же: координационная связь — это НЕвалентная связь.
Ещё важная цитата: «§ 42. Комплексные соединения. Координационная теория Вернера. К началу 90−х годов прошлого столетия был накоплен большой материал по особой группе молекулярных соединений, состав которых не находил объяснений с позиций классической теории валентности. Соединения типа BF3, CH4, NH3, H2O, CO2 и др., в которых элемент проявляет свою обычную максимальную валентность, называются валентно−насыщенными соединениями или соединениями первого порядка. При взаимодействии соединений первого порядка друг с другом получаются соединения высшего порядка. К соединениям высшего порядка относятся гидраты, аммиакаты, продукты присоединения кислот, органических молекул, двойные соли и многие другие. Вот некоторые примеры образования соединений высшего порядка:
CoCl3 + 6NH3 = CoCl3•6NH3
BF3 + HF = BF3•HF
Fe(CN)3 + 3KCN = Fe(CN)3•3KCN» [Угай Я.А. Общая химия: Учебник для студентов хим. спец. ун−тов. — 2−е изд., перераб. и доп. — М.: Высш. шк., 1984. — 440 с., ил.].
И ещё раз про мистера Вернера. Вот здесь:
http://djht.ru/15history/90.html
дан интересный исторический очерк о его представлениях с важными его цитатами. ВАЖНО, что Вернер прекрасно понимал, что связь в комплексах НЕвалентная, и поэтому, чтобы её ОТЛИЧАТЬ от валентной, он дал ей новое название: «побочная валентность». «Подобно тому, — отмечал А. Вернер, — как число, выражающее главную валентность элемента, определяется количеством одновалентных атомов или атомных групп, могущих с ним соединиться (точнее, соединиться с его атомом), — число, выражающее побочную валентность элемента, определяется количеством молекул, могущих вступить в соединение с его атомом». То есть Вернер опять же делил валентные и комплексные соединения как атомные и межмолекулярные (а между МОЛЕКУЛАМИ — связь НЕвалентная, то есть «побочная валентность»).
Считать, что ионные, ковалентные и металлические связи создаются валентными электронами, а продукт этого взаимодействия называется молекулой, — это классическая теория валентной связи. Соответственно, границы молекулы — это когда ВСЕ связи в соединении либо ионные, либо ковалентные, либо металлические — это ВАЛЕНТНЫЕ соединения, то есть «соединения первого порядка». А вот продукты слипания двух или более молекул — это КОМПЛЕКСНЫЕ соединения («соединения высшего порядка»). То есть HBrO4 — это валентное соединение, и это — одна молекула. А HBF4 — это две молекулы (HF и BF3; бор — трёхвалентен), то есть это КОМПЛЕКС молекул = АССОЦИАТ молекул, склеенный «нехимической» связью. И это — классическая химия, а не «новая теория невежды антихимика»!!
И в заключение про CO. Если бы связь в угарном газе былà такая: «C≡O», то, во−первых, тут заведомо невозможные трёхвалентный кислород и трёхвалентный углерод (свободный ион или радикал?); и, во−вторых, если бы связь в карбонилах былà такой «M—C≡O», то при их гидролизе получался бы гидроксид M—OH и кислота H—C≡O! Вас не смущает, что это — полформальдегида? А теперь представьте, что в изонитрилах — четверная связь и пятивалентный аммонийный азот; а в угарном газе тоже четверная связь и оксониевый четырёхвалентный кислород. Сразу ВСЁ объясняется!!! И то, что это — нейтральные молекулы, а не димеры, свободные радикалы, ионы или карбены. И то, что они образуют именно КОМПЛЕКСЫ молекул (молекулярные соединения, ассоциаты), «налипая» на атом металла, как вода в гидратах. ПОЧЕМУ они именно углеродом липнут к металлу? Да потому что это ДИПОЛИ, как и вода, а на углероде — ОТРИЦАТЕЛЬНЫЙ заряд, потому что кислород или азот — онийный и положительный!! Поэтому карбонилы — это НЕ сòли H—C≡O,
Вас не смущает, что это — полформальдегида? А теперь представьте, что в изонитрилах — четверная связь и пятивалентный аммонийный азот; а в угарном газе тоже четверная связь и оксониевый четырёхвалентный кислород. Сразу ВСЁ объясняется!!! И то, что это — нейтральные молекулы, а не димеры, свободные радикалы, ионы или карбены. И то, что они образуют именно КОМПЛЕКСЫ молекул (молекулярные соединения, ассоциаты), «налипая» на атом металла, как вода в гидратах. ПОЧЕМУ они именно углеродом липнут к металлу? Да потому что это ДИПОЛИ, как и вода, а на углероде — ОТРИЦАТЕЛЬНЫЙ заряд, потому что кислород или азот — онийный и положительный!! Поэтому карбонилы — это НЕ сòли H—C≡O,  а подобие гидратов.
а подобие гидратов.
Некоторые определения координационного соединения
1. Первая попытка классификации, включающей в себя комплексные соединения, заключалась в рассмотрении их с позиций соблюдения или несоблюдения правил формальной валентности. При этом соединения подразделялись на два класса — простые (атомные) и комплексные (молекулярные).
Вследствие того, что в комплексном соединении АВ исходные атомные соединения А и В сохраняют свою индивидуальность, считалось, что комплексы не могут переходить без разложения в парообразное состояние. Однако данная классификация перестала быть актуальной после 1893 гòда, когда был получен ряд соединений, не разлагавшихся при переходе в парообразное состояние. Тезис о сохранении индивидуальности исходных компонентов в комплексе был необходим для того, чтобы к координационным не относились такие соединения, как, например, серная кислота, получаемая по реакции соединения двух атомных соединений SO3 и Н2О.». Ниже приводится таблица, которую я в виде картинки приложил сюда: Заметьте, что именно позиции из этой таблицы я здесь (ужè столько времени) объясняю. Далее в этом учебнике приводятся определения, которые давались позже, и их заслуженная критика. Мне нравится определение, которое в 1933 годỳ (через 40 лет ПОСЛЕ Вернера) дал Ф. Файгль: «координационное соединение — это соединение, строение которого не может быть объяснено нормальным числом валентных связей».
Следует подчеркнуть важный факт: ИОННЫЕ и КОВАЛЕНТНЫЕ соединения де−факто имеют одну природу и различаются лишь СТЕПЕНЬЮ ионности, которая, как правило, тем выше — чем больше разница между соединёнными атомами; например, LiF ионнее BeO, который ионнее BN. Кроме того, «Известно, что ионная и ковалентная связи, а также ковалентная и металлическая не имеют резкого разграничения и может наблюдаться переход от одного вида связи к другому.» [И.Я. Клинов. Коррозия химической аппаратуры и коррозионностойкие материалы. Машиностроение. Москва. 1967].
Ещё цитата: «Комплексным соединением называется соединение высшего порядка, образующееся из соединений первого порядка без образования новых электронных пар, а за счёт проявления хотя бы одной координативной связи.» [Я.И. Михайленко. Курс общей и неорганической химии. Высшая школа. Москва 1966. Стр. 119]. То есть опять же: есть МОЛЕКУЛЫ — это соединения первого порядка, то есть ВАЛЕНТНЫЕ соединения, склеенные только валентными электронами; а есть ассоциаты — продукты налипания одной молекулы на другую, и эта межмолекулярная связь «ненастоящая», НЕвалентная.
Вас возмущает «рисование чёрточек» применительно к ионной связи, но почему тогда Вас не возмущают эти чёрточки в CIF−файлах структур алюминатов; ведь кристаллическая решётка сапфира считается ионной? А теперь факт: в структурных формулах металлохелатов ПРИНЯТО рисовать ИОННЫЕ связи чёрточками, а вот комплексные связи в них рисуют СТРЕЛКАМИ! Пример из всё того же учебника:

Надеюсь, Вы не будете доказывать, что связь меди в её енолятах неионная.
Из Химической энциклопедии: «КООРДИНАЦИOННАЯ СВЯЗЬ, хим. связь в комплексных соединениях, в к−рых один или неск. атомов образуют большее число связей, чем допускает высшая формальная валентность этих атомов.» — опять же: координационная связь — это НЕвалентная связь.
Ещё важная цитата: «§ 42. Комплексные соединения. Координационная теория Вернера. К началу 90−х годов прошлого столетия был накоплен большой материал по особой группе молекулярных соединений, состав которых не находил объяснений с позиций классической теории валентности. Соединения типа BF3, CH4, NH3, H2O, CO2 и др., в которых элемент проявляет свою обычную максимальную валентность, называются валентно−насыщенными соединениями или соединениями первого порядка. При взаимодействии соединений первого порядка друг с другом получаются соединения высшего порядка. К соединениям высшего порядка относятся гидраты, аммиакаты, продукты присоединения кислот, органических молекул, двойные соли и многие другие. Вот некоторые примеры образования соединений высшего порядка:
CoCl3 + 6NH3 = CoCl3•6NH3
BF3 + HF = BF3•HF
Fe(CN)3 + 3KCN = Fe(CN)3•3KCN» [Угай Я.А. Общая химия: Учебник для студентов хим. спец. ун−тов. — 2−е изд., перераб. и доп. — М.: Высш. шк., 1984. — 440 с., ил.].
И ещё раз про мистера Вернера. Вот здесь:
http://djht.ru/15history/90.html
дан интересный исторический очерк о его представлениях с важными его цитатами. ВАЖНО, что Вернер прекрасно понимал, что связь в комплексах НЕвалентная, и поэтому, чтобы её ОТЛИЧАТЬ от валентной, он дал ей новое название: «побочная валентность». «Подобно тому, — отмечал А. Вернер, — как число, выражающее главную валентность элемента, определяется количеством одновалентных атомов или атомных групп, могущих с ним соединиться (точнее, соединиться с его атомом), — число, выражающее побочную валентность элемента, определяется количеством молекул, могущих вступить в соединение с его атомом». То есть Вернер опять же делил валентные и комплексные соединения как атомные и межмолекулярные (а между МОЛЕКУЛАМИ — связь НЕвалентная, то есть «побочная валентность»).
Считать, что ионные, ковалентные и металлические связи создаются валентными электронами, а продукт этого взаимодействия называется молекулой, — это классическая теория валентной связи. Соответственно, границы молекулы — это когда ВСЕ связи в соединении либо ионные, либо ковалентные, либо металлические — это ВАЛЕНТНЫЕ соединения, то есть «соединения первого порядка». А вот продукты слипания двух или более молекул — это КОМПЛЕКСНЫЕ соединения («соединения высшего порядка»). То есть HBrO4 — это валентное соединение, и это — одна молекула. А HBF4 — это две молекулы (HF и BF3; бор — трёхвалентен), то есть это КОМПЛЕКС молекул = АССОЦИАТ молекул, склеенный «нехимической» связью. И это — классическая химия, а не «новая теория невежды антихимика»!!
И в заключение про CO. Если бы связь в угарном газе былà такая: «C≡O», то, во−первых, тут заведомо невозможные трёхвалентный кислород и трёхвалентный углерод (свободный ион или радикал?); и, во−вторых, если бы связь в карбонилах былà такой «M—C≡O», то при их гидролизе получался бы гидроксид M—OH и кислота H—C≡O!
У вас нет необходимых прав для просмотра вложений в этом сообщении.
Ивана Царевича от ВЗРОСЛЫХ братьев отличает НЕ гениальность, а девственность. Подоночность, серость, тупость и пассивность — это НЕ врождённая бездарность, а НЕРЕСТОВЫЕ изменения, именуемые в мире рыб ЛОШАНИЕМ, а в мире людей СТЕПЕННОСТЬЮ и ВЗРОСЛОСТЬЮ. ©
Re: Спор о фазах, природе химической связи, валентности и степени окисления
Avak_Avakyan
У вас мозг рака!!!
У вас мозг рака!!!
Либо это новая теория невежды с кашей в голове вместо базовых знаний, либо толстый троллинг. В антихимию, быстро, решительно!HBF4 — это две молекулы (HF и BF3; бор — трёхвалентен), то есть это КОМПЛЕКС молекул = АССОЦИАТ молекул, склеенный «нехимической» связью. И это — классическая химия, а не «новая теория невежды антихимика»!!
Когда начинает изменять память, практики заводят записную книжку, а романтики садятся писать мемуары.
- Droog_Andrey
- Сообщения: 2699
- Зарегистрирован: Сб сен 29, 2007 8:29 pm
- Контактная информация:
Re: Спор о фазах, природе химической связи, валентности и степени окисления
Не прощу.
Не-а. Это не высшая, а четвёртая МО.
Интегралы перекрывания и т.п. - это всё равно в некоторой степени произвол, ибо в молекуле нет АО. Можно, конечно, качественно оценить вклад. Вот, например, вклад C2s в ВЗМО довольно невелик. Но отождествлять молекулярные состояния с атомными - разве что для core electrons прокатит, а в валентной области - увольте
2^74207281-1 is prime!
- Avak_Avakyan
- Сообщения: 95
- Зарегистрирован: Пн июн 15, 2015 10:08 pm
Re: Спор о фазах, природе химической связи, валентности и степени окисления
Я привёл официальные учебники, причём достаточно нестарые. Заметьте, что учебник 1984 гòда для университетских химиков студентов [Угай Я.А. Общая химия: Учебник для студентов хим. спец. ун−тов. — 2−е изд., перераб. и доп. — М.: Высш. шк., 1984. — 440 с., ил.] — позволяет себе запись формул, явно «еретическую» с Вашей точки зрения:
«BF3 + HF = BF3•HF
Fe(CN)3 + 3KCN = Fe(CN)3•3KCN»,
и рассматривает комплексные соединения именно как ассоциаты молекул (даже формулы так записаны), склеенные невалентной связью.
Понимаете ли, батенька: если учебники кажутся «антихимией» тому, кто их недоучил, — то из этого не следует, что содержание этих учебников является «новой теорией невежды».
Ивана Царевича от ВЗРОСЛЫХ братьев отличает НЕ гениальность, а девственность. Подоночность, серость, тупость и пассивность — это НЕ врождённая бездарность, а НЕРЕСТОВЫЕ изменения, именуемые в мире рыб ЛОШАНИЕМ, а в мире людей СТЕПЕННОСТЬЮ и ВЗРОСЛОСТЬЮ. ©
Re: Спор о фазах, природе химической связи, валентности и степени окисления
Экий Вы мстительный, коллега!
Посмотрите приложенную статью, табл. II "SCF orbitals and orbital energies for CO" на с. 1196. Видите состояние ф6сигма с энергией +0.86? Которое включает +0.98106(C2s)-1.14162(O2s)?
Вот оно разрыхляющее, и высшее по энергии, с него и происходит ионизация, которая приводит к сокращению длины связи.
Согласен! Но ведь оценить можно даже количественно, и используя интегралы перекрывания -- довольно точно, и семи пядей во лбу для этого быть не надо!Droog_Andrey писал(а): ↑Пт май 11, 2018 12:27 pmИнтегралы перекрывания и т.п. - это всё равно в некоторой степени произвол, ибо в молекуле нет АО. Можно, конечно, качественно оценить вклад. Вот, например, вклад C2s в ВЗМО довольно невелик. Но отождествлять молекулярные состояния с атомными - разве что для core electrons прокатит, а в валентной области - увольте
У вас нет необходимых прав для просмотра вложений в этом сообщении.
When you open your heart to patriotism, there is no room for prejudice.
Re: Спор о фазах, природе химической связи, валентности и степени окисления
Ну можно и открыть... Только сначала надо понять, что мы изучаем -- химию или историю?Avak_Avakyan писал(а): ↑Пт май 11, 2018 1:01 amОх…Итак, давайте откроем УЧЕБНИКИ…
...
ИСТОРИЯ КООРДИНАЦИОННОЙ ХИМИИ
...
Первая попытка классификации, включающей в себя комплексные соединения
...
Ниже приводится таблица, которую я в виде картинки приложил сюда:
..."Первая классификация соединений, включающая понятие "комплекс"
...
«Комплексным соединением называется соединение высшего порядка, образующееся из соединений первого порядка без образования новых электронных пар, а за счёт проявления хотя бы одной координативной связи.» [Я.И. Михайленко. Курс общей и неорганической химии. Высшая школа. Москва 1966. Стр. 119]. То есть опять же: есть МОЛЕКУЛЫ — это соединения первого порядка, то есть ВАЛЕНТНЫЕ соединения, склеенные только валентными электронами; а есть ассоциаты — продукты налипания одной молекулы на другую, и эта межмолекулярная связь «ненастоящая», НЕвалентная.
Если историю, то всё верно: были такие воззрения, был херр Вернер, да и комплексные соединения вполне себе можно называть ассоциатами (как и любые другие соединения). Ну чем H2O -- не ассоциат двух атомов водорода с одним атомом кислорода? Всё это было, было, было, но прошло.
А вот если изучать химию, то стоит открыть учебники посерьёзнее, например:
Коттон Ф., Уилкинсон Дж. Современная неорганическая химия. М.: Мир, 1969.
Кольдиц Л. (Ред.) Анорганикум. М.: Мир, 1984.
Уэллс А. Структурная неорганическая химия. М.:Мир, 1987.
Третьяков Ю. Д. (ред.) Неорганическая химия. В трёх томах. М.: Академия, 2004.
Если хочется реально понять координационную химию, то надо читать специализированную литературу:
Киселёв Ю.М., Добрынина Н.А. Химия координационных соединений. М.: Академия, 2007.
Wilkinson G. (Ed.) Comprehensive coordination chemistry (in 7 vol.) Pergamon press, 1987.
McCleverty J. (Ed.) Comprehensive coordination chemistry II (in 10 vol.) Elsevier, 2005.
После прочтения, наверное, будет, что обсудить. А так -- скучно!
Нет, оксиды алюминия вполне себе ковалентно-связанные. См. прикреплённую статью. Ионные связи в формулах никогда не рисуют чёрточками, а ставят знаки + и - без указания даже приблизительного пространственного расположения ионов, т.к. ионная связь по определению -- ненаправленная и ненасыщаемая.Avak_Avakyan писал(а): ↑Пт май 11, 2018 1:01 amВас возмущает «рисование чёрточек» применительно к ионной связи, но почему тогда Вас не возмущают эти чёрточки в CIF−файлах структур алюминатов; ведь кристаллическая решётка сапфира считается ионной? А теперь факт: в структурных формулах металлохелатов ПРИНЯТО рисовать ИОННЫЕ связи чёрточками, а вот комплексные связи в них рисуют СТРЕЛКАМИ!
Нет, не смущает, потому что такой фантастической кислоты всё равно не существует, а вот про строение молекулы CO есть вполне обстоятельная статья:Avak_Avakyan писал(а): ↑Пт май 11, 2018 1:01 amИ в заключение про CO. Если бы связь в угарном газе былà такая: «C≡O», то, во−первых, тут заведомо невозможные трёхвалентный кислород и трёхвалентный углерод (свободный ион или радикал?); и, во−вторых, если бы связь в карбонилах былà такой «M—C≡O», то при их гидролизе получался бы гидроксид M—OH и кислота H—C≡O!Вас не смущает, что это — полформальдегида?
Мне столько не выпить, чтобы представить себе пятивалентный азотAvak_Avakyan писал(а): ↑Пт май 11, 2018 1:01 amА теперь представьте, что в изонитрилах — четверная связь и пятивалентный аммонийный азот; а в угарном газе тоже четверная связь и оксониевый четырёхвалентный кислород. Сразу ВСЁ объясняется!!!
Да и с четырёхвалентным кислородом туговато
Понятно что карбонилы -- это не соли, потому что соли -- ионные соединения, а в карбонилах связь ковалентная, образованная по донорно-акцепторному механизму.Avak_Avakyan писал(а): ↑Пт май 11, 2018 1:01 amПоэтому карбонилы — это НЕ сòли H—C≡O,а подобие гидратов.[/color]
У вас нет необходимых прав для просмотра вложений в этом сообщении.
When you open your heart to patriotism, there is no room for prejudice.
Re: Спор о фазах, природе химической связи, валентности и степени окисления
Напоминает "Письмо к учёному соседу" А. П. Чехова.
When you open your heart to patriotism, there is no room for prejudice.
- Droog_Andrey
- Сообщения: 2699
- Зарегистрирован: Сб сен 29, 2007 8:29 pm
- Контактная информация:
Re: Спор о фазах, природе химической связи, валентности и степени окисления
А ничего, что там вклад 2p больше, чем 2s?
Ну и статья старовата. Я вот считаю CASSCF и вижу, что вклад C2s в четвёртую МО намного выше, чем в ВЗМО
Количественные оценки бессмысленны, ибо, опять таки, атомных орбиталей в молекулах в валентной области нет
2^74207281-1 is prime!
- Droog_Andrey
- Сообщения: 2699
- Зарегистрирован: Сб сен 29, 2007 8:29 pm
- Контактная информация:
Re: Спор о фазах, природе химической связи, валентности и степени окисления
Да ладно. Присмотритесь к основному ацетату бериллия, в виде которого обычно бериллий в лабе появляется
2^74207281-1 is prime!
Re: Спор о фазах, природе химической связи, валентности и степени окисления
Согласен, чёрт с ним, 2s или 2p преобладает. Суть в том, что у CO верхнее занятое состояние (вероятность ионизации которого наибольшая) разрыхляющее, а у N2 -- связывающее.
Просто у меня в лабе сульфат, я смотрел, смотрел в банку, так и не заметил четвёртой связи у кислорода. А про ацетат согласен. Ещё из той же оперы ацетат алюминия, вроде как. Конечно, во втором периоде валентность 4 -- наивысшая возможная. Всё-таки с кислородом такое редко случается, мешает сильно проваленная 2s. Не то, что у бора, углерода или азота, для которых 4 -- самая типичная валентность.Droog_Andrey писал(а): ↑Пт май 11, 2018 4:38 pmДа ладно. Присмотритесь к основному ацетату бериллия, в виде которого обычно бериллий в лабе появляется
When you open your heart to patriotism, there is no room for prejudice.
- Avak_Avakyan
- Сообщения: 95
- Зарегистрирован: Пн июн 15, 2015 10:08 pm
Re: Спор о фазах, природе химической связи, валентности и степени окисления
Ну что ж; проспитесь, и
И вот ещё: «Азот имеет:
валентность 2 в NO
валентность 3 в NH3
валентность 4 в NO2
валентность 5 в HNO3» [И. Нентвиг. Химический тренажер. Ч. 1. Пер с англ. М: Мир, 1986. Стр. 340].
Ранее я ужè давал ссылку на учебник 2008 гòда, где перечислены разнообразные определения понятия «валентность» разных авторов, многие из которых радикально противоречат друг другу. Я понимаю, что Вам нравится только узкий круг той литературы, где определения и понятия используются в нравящемся Вам нетрадиционном значении. Химики же вроде меня, привыкшие использовать термины в их традиционном значении, просто видят, что у Вас всё не то.
Я привожу не только питекантропскую древность, а учебники и справочники девяностых, по которым я сам учился, и которые представляют собой базовые основы химических знаний.
А главное в Вам нравящихся определениях — это неразличение простых и комплексных соединений. Я ужè говорил традиционное определение: есть простые (атомные) и комплексные (молекулярные) соединения. Атомные соединены валентными электронами; а молекулы друг к дружке тяготеют за счёт «остаточных» невалентных сил. И это НЕ просто «косяки классификаций», а радикальное отличие поведения в химреакциях. Калий с угарным газом реагирует валентно, образуя НЕ комплекс, а простые соединения, где приобретает степень окисления. По количественному составу эти продукты близки к карбонилам (сòли дигидроксиацетилена, гексагидроксибензола, кроконаты), но с кислотами они выделяют соответствующие оксоуглеродные кислòты. А вот железо с угарным газом образует молекулярные ассоциаты (карбонилы), НЕ обретает степень окисления, и кислоты дают с карбонилами водород и угарный газ, то есть угарный газ просто отваливается, как гидратная вода, а железо реагирует, как само по себе. Как бы ни былà похожа связь CO с Fe в карбонилах на ковалентную на спектрометре, она ХИМИЧЕСКИ ВЕДЁТ СЕБЯ радикально иначе, чем связь C—C в этане: например, даже если порвать её физическим воздействием, этан не превратится в «молекулы CH3».
Только то узкое направление нетрадиционалистов, которое нравится лично Вам.
Нет, «В работе исследовались мишени сапфира Al2O3, кристаллическая решётка которого образована ионами Al3+ и O2−. … Тип связей в Al2O3 преимущественно ионный. Доля ковалентных связей составляет ~ 20 %. Электронная энергетическая структура сапфира типична для ионных кристаллов.» [И.А. Афанасьева, В.В. Бобков, … Влияние модификации поверхности сапфира при ионном облучении на выход возбуждённых частиц].
Рисуют повсеместно; достаточно набрать в картинках Гугла, например, «глицинат меди»:

В хелатах: ионная связь — чёрточками; невалентная (молекулярная) связь — стрелочками. Опять же, это — традиционные ценности, скрепы.
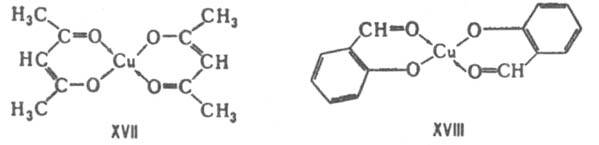
И где Вы такие «определения» находите?
ПОТОМУ И не существует, что не может существовать трёхвалентный кислород, и потому что связь с железом НЕвалентная.
Ацетилен назвать ионным — язык не поворачивается; он именно ковалентный. Но калий реагирует с ним как с кислотой, вытесняя водород. Метан — ВААЩЕ эталон ковалентности; но алюминий делает с ним (при высокой температуре) соль Al4C3. Но в том−то и заключается принципиальная разница, которую Вы абсолютистски не хотите видеть, между валентными соединениями и соединениями с невалентной связью (назовёте ли Вы её донорно−акцепторной, ван−дер−ваальсовой или марсианской): и Na2C2, и Al4C3, и Mg2C3 при гидролизе выделяют соответствующий углеводород (играющий роль кислоты в этих карбидах); а вот соединения графита со щелочными металлами (С8М, С16М, С24М, С36М, С40М, С64М) при гидролизе выделяют только водород, что указывает на то, что ВАЛЕНТНОЙ («химической») связи между металлом и углеродом в них НЕТ!! В ЭТОМ радикальная разница между «реальными» (валентными) соединениями, и ассоциатами молекул. Щелочные металлы чуть ли не со всем и вся «рады» образовывать ионные сòли, но — с графитом у них получаются лишь клатраты (как Fe3C).
Ивана Царевича от ВЗРОСЛЫХ братьев отличает НЕ гениальность, а девственность. Подоночность, серость, тупость и пассивность — это НЕ врождённая бездарность, а НЕРЕСТОВЫЕ изменения, именуемые в мире рыб ЛОШАНИЕМ, а в мире людей СТЕПЕННОСТЬЮ и ВЗРОСЛОСТЬЮ. ©
- Droog_Andrey
- Сообщения: 2699
- Зарегистрирован: Сб сен 29, 2007 8:29 pm
- Контактная информация:
Re: Спор о фазах, природе химической связи, валентности и степени окисления
Ну так это просто завуалированное (и сомнительно формализованное) изначальное утверждение:
Droog_Andrey писал(а): ↑Вт май 08, 2018 11:48 pmЧто интересно, при ионизации CO связь укорачивается (в отличие от N2). Что как бы намекает, что связь не такая уж и тройная
2^74207281-1 is prime!
- Droog_Andrey
- Сообщения: 2699
- Зарегистрирован: Сб сен 29, 2007 8:29 pm
- Контактная информация:
Re: Спор о фазах, природе химической связи, валентности и степени окисления
Ещё более проваленная 6s у висмута не мешает тетрафенилвисмутонию быть вполне устойчивым
2^74207281-1 is prime!
Re: Спор о фазах, природе химической связи, валентности и степени окисления
Примерно что-то подобное я и ожидал увидеть. В смысле, 1930.Avak_Avakyan писал(а): ↑Сб май 12, 2018 12:31 amНу что ж; проспитесь, ина свежую голову откройте учебник: «Амины суть производные аммиака, в котором водород замещён на углеводородные радикалы. … В этих соединениях азот трёхвалентен; но известно, что он может функционировать ещё и как пятивалентный элемент, например в соединениях NH4Cl или NH4•OH; между органическими азотистыми телами есть также содержащие пятивалентный азот, например (CH3)4N•OH; эти соединения суть производные гидроокиси аммония NH4•OH, в котором четыре атома водорода замещены на четыре углеводородных радикала» [Проф. С.Н. Реформатский. Начальный курс органической химии. Москва−Ленинград 1930].
К сожалению, подобные старые представления всё ещё бродят по современным публикациям, авторы которых не удосуживаются изучить современное состояние дел в химии, а просто переписывают допотопные тексты. Всё это прискорбно, скучно и совершенно неактуально.
Видите ли, современная химия ушла от этих древностей так далеко, что с высоты сколько--нибудь серьёзной химической науки всей этой "пыли веков" просто не видно.
When you open your heart to patriotism, there is no room for prejudice.
Re: Спор о фазах, природе химической связи, валентности и степени окисления
Изначальное утверждение представляет собой экспериментальный факт, а данное пояснение -- его теоретическое объяснение. А то, что одно соответствует другому -- так и должно быть.Droog_Andrey писал(а): ↑Сб май 12, 2018 6:55 pmНу так это просто завуалированное (и сомнительно формализованное) изначальное утверждение:Droog_Andrey писал(а): ↑Вт май 08, 2018 11:48 pmЧто интересно, при ионизации CO связь укорачивается (в отличие от N2). Что как бы намекает, что связь не такая уж и тройная
По поводу кратности связи мы уже, вроде бы, пришли к взаимопониманию, что кратность связи, как и валентность -- понятия условные и приблизительные.
Не согласен, Bi6s лежат примерно при 14 эВ, а O2s -- около 22-23. И тот, и другой уровень, в сущности, остовные, и в связи не участвуют (см. фиг. 1, 3, 5 в прикреплённой статье). Спектр тетрафенилвисмутония я ни разу не видел, но думаю, связи там примерно такие же, как в боразоне или в алмазе, в которых s-состояния вроде как чисто формально и участвуют, но в действительности вклад их невелик (см. прикреплённую статью). (Это всё к развенчиванию вредной теории о мифической "sp3-гибридизации".)Droog_Andrey писал(а): ↑Сб май 12, 2018 7:08 pmЕщё более проваленная 6s у висмута не мешает тетрафенилвисмутонию быть вполне устойчивым
У вас нет необходимых прав для просмотра вложений в этом сообщении.
When you open your heart to patriotism, there is no room for prejudice.
Кто сейчас на конференции
Сейчас этот форум просматривают: нет зарегистрированных пользователей и 25 гостей