Корреляции и их наклон между pK соединений в полярных и неполярных растворителях
Корреляции и их наклон между pK соединений в полярных и неполярных растворителях
Я пытаюсь квантово-химически предсказывать pKa кислот и фенолов, и обнаружил, что с более тщательным учётом сольватации угол наклона корреляции между энергией депротонирования и экспериментальной pKa становится ближе к теоретическому. Мне надо это понятно объяснить в публикации. Как вы думаете, верно ли такое рассуждение:
Сильные кислоты содержат более полярные фрагменты OH (имеется в виду нейтральная форма), поэтому сильные кислоты в нейтральной форме сильнее стабилизируются в полярных растворителях, чем в неполярных. Как следствие, в полярных растворителях, по сравнению с неполярными, сильные кислоты становятся немного слабее, а слабые немного сильнее.
Верно ли это утверждение? Если взять ряд кислот и померить их pKa в воде и неполярных растворителях, получится ли, что полярный растворитель немного уменьшает зависимость pKa от свойств самих молекул, т.е. в полярных растворителях сильные кислоты становятся чуть слабее, а слабые чуть сильнее из-за растворителя?
Сильные кислоты содержат более полярные фрагменты OH (имеется в виду нейтральная форма), поэтому сильные кислоты в нейтральной форме сильнее стабилизируются в полярных растворителях, чем в неполярных. Как следствие, в полярных растворителях, по сравнению с неполярными, сильные кислоты становятся немного слабее, а слабые немного сильнее.
Верно ли это утверждение? Если взять ряд кислот и померить их pKa в воде и неполярных растворителях, получится ли, что полярный растворитель немного уменьшает зависимость pKa от свойств самих молекул, т.е. в полярных растворителях сильные кислоты становятся чуть слабее, а слабые чуть сильнее из-за растворителя?
Re: Корреляции и их наклон между pK соединений в полярных и неполярных растворителях
что значит "сильнее - слабее"?
ПС как вы представляете диссоциацию фенола в тетрахлоруглероде?
Не красота спасёт мир, а транквилизаторы.
Re: Корреляции и их наклон между pK соединений в полярных и неполярных растворителях
Сорри, про тетрахлоруглерод ничего сказать не могу, но мой вопрос очень простой - как коррелируют величины pK кислот в полярных и неполярных растворителях (интересует прежде всего угол наклона этой корреляции).
Re: Корреляции и их наклон между pK соединений в полярных и неполярных растворителях
у меня есть подозрение, что вам кажется, что вы задаете простой вопрос про растворимость, сольватацию, диссоциацию и что считать кислотой в неполярном растворителе. но это только мое мнение
Не красота спасёт мир, а транквилизаторы.
Re: Корреляции и их наклон между pK соединений в полярных и неполярных растворителях
Ну это нормальная формулировка, скажем "в каком из данных растворителей ацетиленовый протон кислее" (константа равновесия выше/ниже)
Re: Корреляции и их наклон между pK соединений в полярных и неполярных растворителях
"кислее" это та, где дипольный момент больше? а равновесие между чем и чем? а как быть, допустим, с раствором тетрайодида германия в тетрахлоруглероде, где в качестве кислоты выступает йодид-ион?
понятно, что ТС "заужает" проблематику до угольной кислоты в воде, но вопрос что такое "слабая кислота" и "сильная кислота" в неполярном растворителе остается для меня неясным.
Не красота спасёт мир, а транквилизаторы.
Re: Корреляции и их наклон между pK соединений в полярных и неполярных растворителях
Нет, кислее там где равновесие сильнее смещено в диссоциированную форму.
Re: Корреляции и их наклон между pK соединений в полярных и неполярных растворителях
в неполярном растворителе?
Не красота спасёт мир, а транквилизаторы.
Re: Корреляции и их наклон между pK соединений в полярных и неполярных растворителях
я не совсем понимаю что вас смущает в неполярном растворителе...
Тупо пара результатов с самого тупого запроса в гугл.
https://pubs.acs.org/doi/full/10.1021/jo9713013
Acid−Base Equilibria in Nonpolar Media. 1. A Spectrophotometric Method for Acidity Measurements in Heptane
(за ним последовали еще несколько частей, например https://pubs.acs.org/doi/10.1021/jo0343477 с таблицами)
https://pubs.rsc.org/en/content/article ... c5py01157d
Acid–base indicators for non-polar solvents via anion-exchange of polymeric ionic liquids with anionic dyes
Re: Корреляции и их наклон между pK соединений в полярных и неполярных растворителях
а смущает меня отсутствие свободного протона в растворителе (или я не так понял?)
Не красота спасёт мир, а транквилизаторы.
Re: Корреляции и их наклон между pK соединений в полярных и неполярных растворителях
Ааа, я начал понимать что вам не нравится.
1) кислотность и диссоциация протона от кислотного остатка не означают наличия "свободного" протона. В вышеприведенных статьях для измерения кислотности в гептане используются основания. Наиболее тупо см https://pubs.rsc.org/en/content/article ... c8cp02349b
2) некоторые неполярные растворители типа бензола хорошими кислотами тупо протонируются
3) наконец худо-бедно протон всетаки сольватируется. Энтальпию можно посчитать и поумнее чем у https://www.google.com/url?sa=t&source= ... OI0IsbQcaP (осторожно, ссылка напрямую на документ) но это не суть. Опять же вопрос что мы называем неполярными растворителями, те которые за чертой 15, или молекулы которых не имеют дипольного момента. К первым например относится дихлорметан, я думаю слабые галогеновые связи могут построить вокруг протона вполне приличную сольватную шубу.
1) кислотность и диссоциация протона от кислотного остатка не означают наличия "свободного" протона. В вышеприведенных статьях для измерения кислотности в гептане используются основания. Наиболее тупо см https://pubs.rsc.org/en/content/article ... c8cp02349b
2) некоторые неполярные растворители типа бензола хорошими кислотами тупо протонируются
3) наконец худо-бедно протон всетаки сольватируется. Энтальпию можно посчитать и поумнее чем у https://www.google.com/url?sa=t&source= ... OI0IsbQcaP (осторожно, ссылка напрямую на документ) но это не суть. Опять же вопрос что мы называем неполярными растворителями, те которые за чертой 15, или молекулы которых не имеют дипольного момента. К первым например относится дихлорметан, я думаю слабые галогеновые связи могут построить вокруг протона вполне приличную сольватную шубу.
Re: Корреляции и их наклон между pK соединений в полярных и неполярных растворителях
Я на самом деле не очень в курсе - если например в CCl4 поместить уксусную кислоту, она будет диссоциировать с образованием например HCCl4+? Если CCl4 или бензол неудачные примеры, может быть можно назвать промежуточные - менее полярные, чем вода, но в которых можно померить pK.
Re: Корреляции и их наклон между pK соединений в полярных и неполярных растворителях
все верно, но я к тому, что проблема сложнее, чем кажется ТС
ПС я тут подумал, про в статье выясняли кислота это или основание по контрольному веществу, а гексан брали чтобы минимизировать его влияние в силу его неполярности
Последний раз редактировалось bigM Пт ноя 04, 2022 12:31 pm, всего редактировалось 1 раз.
Не красота спасёт мир, а транквилизаторы.
Re: Корреляции и их наклон между pK соединений в полярных и неполярных растворителях
проблема в том, что померить константу диссоциации сложно не вводя новых веществ, которые тоже надо будет учитывать в расчётах.Vit Nhoc писал(а): ↑Пт ноя 04, 2022 11:10 amЯ на самом деле не очень в курсе - если например в CCl4 поместить уксусную кислоту, она будет диссоциировать с образованием например HCCl4+? Если CCl4 или бензол неудачные примеры, может быть можно назвать промежуточные - менее полярные, чем вода, но в которых можно померить pK.
ваш пример очень интересен. даже если уксусная кислота растворится (в каком количестве?) она диссоциировать не будет, но сольватация произойдет (о чем Гесс говорит). для эксперимента надо каким-либо образом "обезводить" уксусную кислоту, в противном случае эту остаточную воду надо учитывать (второй растворитель), т.к. в ней диссоциация будет и проявятся "слабокислотные" свойства уксусной кислоты.
ПС слабыми я бы назвал кислоты/основания, у которых диссоциация (пара растворитель-вещество) зависит от концентрации (в определенном интервале, условно скажем до 50%).
Не красота спасёт мир, а транквилизаторы.
Re: Корреляции и их наклон между pK соединений в полярных и неполярных растворителях
Я пытаюсь найти работы, в которых строятся такие корреляции (между pK в разных растворителях), нашёл пока одну бразильскую: там сравниваются pKa фенолов в воде и CH3CN, корреляция очень чёткая, а её наклон очень отличается от 1: pKa (CH3CN) = 1.68*pKa (water) + 9.80. Т.е. в CH3CN разброс pK больше, чем в воде. Я сходу не понял - это подтверждает или опровергает мою идею, которую я изложил в первом сообщении? Если считать ацетонитрил менее полярным растворителем, чем вода, то как бы подтверждает. Может быть, кроме полярности растворителя есть разные прочие факторы, влияющие на pK в этом растворителе?
Re: Корреляции и их наклон между pK соединений в полярных и неполярных растворителях
Как-то не совсем понятно получается. Вы считаете энергии депротонирования, как разницу энергий нейтральной и депротонированной форм или как-то по-другому? Если как разницу энергий форм, то при стабилизации кислот растворителем нужно учитывать стабилизацию как нейтральной, так и депротонированной форм. Полярность ОН групп - термин не очень подходящий, лучше говорить об энергиях сольватации, а не о полярности. Не уверен, что удастся объединить при этом протонные и апротонные растворители в одну шкалу, механизмы сольватации в них сильно отличаются.Vit Nhoc писал(а): ↑Чт ноя 03, 2022 3:48 pmКак вы думаете, верно ли такое рассуждение:
Сильные кислоты содержат более полярные фрагменты OH (имеется в виду нейтральная форма), поэтому сильные кислоты в нейтральной форме сильнее стабилизируются в полярных растворителях, чем в неполярных. Как следствие, в полярных растворителях, по сравнению с неполярными, сильные кислоты становятся немного слабее, а слабые немного сильнее.
Выражаясь более наукообразно, Вы хотите сказать, что с ростом полярности растворителя сила кислоты увеличивается? Ну, в общем, это обычно так и есть. И именно за счёт лучшей сольватации анионов кислот полярными растворителями. Для нейтральных молекул этот выигрыш в энергии сольватации значительно меньше.Как следствие, в полярных растворителях, по сравнению с неполярными, сильные кислоты становятся немного слабее, а слабые немного сильнее.
Re: Корреляции и их наклон между pK соединений в полярных и неполярных растворителях
Есть у меня подозрение, что работ по сравниванию рКа в разных растворителях можно найти сотни, если не тысячи. Для понимания общей картины десять-двадцать таких работ стоит почитать. Тогда станет понятно, почему сравнение полярности апротонного растворителя с водой, для оценки кислотности тех же фенолов не так важно, как учёт специфической сольватации.Vit Nhoc писал(а): ↑Пн ноя 07, 2022 12:21 pmЯ пытаюсь найти работы, в которых строятся такие корреляции (между pK в разных растворителях), нашёл пока одну бразильскую: там сравниваются pKa фенолов в воде и CH3CN, корреляция очень чёткая, а её наклон очень отличается от 1: pKa (CH3CN) = 1.68*pKa (water) + 9.80. Т.е. в CH3CN разброс pK больше, чем в воде. Я сходу не понял - это подтверждает или опровергает мою идею, которую я изложил в первом сообщении? Если считать ацетонитрил менее полярным растворителем, чем вода, то как бы подтверждает. Может быть, кроме полярности растворителя есть разные прочие факторы, влияющие на pK в этом растворителе?
Re: Корреляции и их наклон между pK соединений в полярных и неполярных растворителях
дипольный момент растворителя - один из факторов сольватации. несомненно его надо учитывать, но он не единственный и не определяющий (вроде бы еще влияют диэлектрическая проницаемость, вязкость, может ещё какие константы). сама по себе задача весьма не тривиальная, в лоб (механистически), как планирует ТС, в общем виде её не решить.
ПС я так думаю ТС, хочет так
Не красота спасёт мир, а транквилизаторы.
Re: Корреляции и их наклон между pK соединений в полярных и неполярных растворителях
Не совсем понял вопрос. Может быть вы имеете в виду, что в полярных растворителях цифра pKa меньше, чем в неполярных? Я это заметил, хотя даже это верно не для всех соединений.Allex' писал(а): ↑Пн ноя 07, 2022 12:35 pmВыражаясь более наукообразно, Вы хотите сказать, что с ростом полярности растворителя сила кислоты увеличивается? Ну, в общем, это обычно так и есть. И именно за счёт лучшей сольватации анионов кислот полярными растворителями. Для нейтральных молекул этот выигрыш в энергии сольватации значительно меньше.
Сейчас я сравниваю pK соединений в воде и метаноле. Найти статьи, где строится такая корреляция, сходу не получилось, поэтому я выписал значения из одной статьи и построил эту корреляцию:
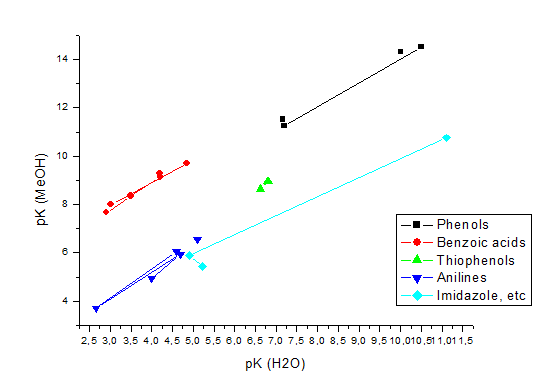
Получается, что для каждого класса соединений эта корреляция своя, ""слишком всё эмпирически".
Правильно ли я понимаю, что вода это более полярный растворитель, чем метанол?
Re: Корреляции и их наклон между pK соединений в полярных и неполярных растворителях
надо сравнить дипольные моменты воды и метанола (иного растворителя), а на счет эмпиричности, здесь, на форуме об этом неоднократно говорили.
Не красота спасёт мир, а транквилизаторы.
Кто сейчас на конференции
Сейчас этот форум просматривают: нет зарегистрированных пользователей и 38 гостей