выберите первую букву в названии статьи:
1-9
А Б В Г Д Е Ж З И К Л М Н О П Р С Т У Ф Х Ц Ч Ш Щ Э Ю Я
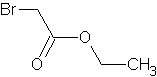
Синонимы:
этилбромацетат
Внешний вид:
бесцветн. жидкость
Брутто-формула (система Хилла): C4H7BrO2
Формула в виде текста: BrCH2COOC2H5
Молекулярная масса (в а.е.м.): 167,01
Температура кипения (в °C): 159
Растворимость (в г/100 г или характеристика):
вода: не растворим
диэтиловый эфир: смешивается
этанол: смешивается
Метод получения 1.
(лабораторный синтез)
Источник информации: "Синтезы органических препаратов" сб.3 М.1952 стр. 504-507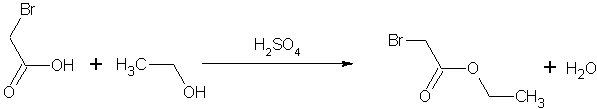 Пары этилового эфира бромуксусной кислоты чрезвычайно раздражающе действуют на глаза. Препарат необходимо хранить в герметически закрытых сосудах и применять в открытой посуде только в хорошо действующем вытяжном шкафу. Для этерификации можно применить отделитель, который устроен так, что более легкая жидкость возвращается в реакционную колбу, а более тяжелую (воду) спускают из нижней части отделителя. Можно пользоваться несколько более простым прибором, в котором отделитель для воды имеет вид, изображенный на рисунке (примечание 7). Неочищенную бромуксусную кислоту помещают в 3-литровую колбу вместе с 610 мл спирта (9,9 моля, избыток) и 950 мл бензола. Для ускорения реакции туда же прибавляют около 1,5 мл концентрированной серной кислоты (примечание 8) и кипятят смесь на водяной бане, причем во время реакции воду из отделителя сливают и измеряют. От бензола отделяется около 296 мл жидкости (состоящей примерно на 50% из спирта и на 50% из воды); в это количество входит вся вода, образующаяся во время реакции, а также избыток спирта. Когда отделение воды от бензола прекратится, к реакционной смеси прибавляют 75 мл спирта и продолжают нагревание в течение получаеа. Если реакция закончена, то дестиллат более не расслаивается. Показателем окончания реакции является также то, что бензол, поступающий из боковой трубки отделителя, становится прозрачным и скорость стекания флегмы из холодильника значительно уменьшается. Количество бензола, которое па этой стадии конденсируется и удаляется через отделитель, составляет 150 мл. Смесь переносят в делительную воронку и промьтают один раз 1500 мл воды, один раз 1500 мл 1%-ного раствора двууглекислого натрия и, наконец, 1 500 мл воды. Затем смесь сушат над безводным сернокислым натрием и фракционируют при атмосферном давлении на масляной бане с применением елочного дефлегматора высотой 30 см (примечание 9). Собирают фракцию, кипящую при 154—155° (759 мм) (примечание 10). Выход составляет примерно 818 г (65—70% теоретич.). Примечания 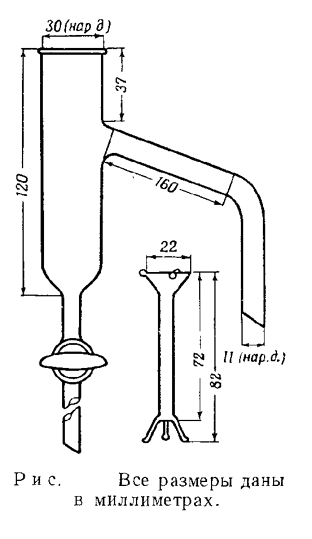 7. Отделитель, показанный на рисунке, является видоизменением этого прибора, применяемого для определения содержания воды по методу Дина и Старка. Размеры отделителя можно изменять в зависимости от индивидуальных целей, поскольку этот вопрос касается главным образом удобства. Отделитель можно применять без внутренней воронки, но при ее наличии (К. Кельш, частное сообщение) конденсат разделяется на два слоя быстро и полностью, причем жидкость, стекающая из холодильника, не вызывает перемешивания обеих фаз в отделителе. Ножка воронки должна быть такой длины, чтобы верхний край воронки находился выше бокового отвода отделителя. Трубку отделителя можно градуировать, однако это не обязательно. 7. Отделитель, показанный на рисунке, является видоизменением этого прибора, применяемого для определения содержания воды по методу Дина и Старка. Размеры отделителя можно изменять в зависимости от индивидуальных целей, поскольку этот вопрос касается главным образом удобства. Отделитель можно применять без внутренней воронки, но при ее наличии (К. Кельш, частное сообщение) конденсат разделяется на два слоя быстро и полностью, причем жидкость, стекающая из холодильника, не вызывает перемешивания обеих фаз в отделителе. Ножка воронки должна быть такой длины, чтобы верхний край воронки находился выше бокового отвода отделителя. Трубку отделителя можно градуировать, однако это не обязательно.
8. В отсутствие катализатора реакция протекает медленнее и выходы получаются меньшими. Серную кислоту можно заменить фосфорной, однако применение серной кислоты дает лучшие выходы в более короткое время. 9. Если не применять дефлегматора, то в головном погоне можно потерять 15—20% вещества. 10. Собирают фракцию, кипящую в пределах одного градуса. В различные дни, в зависимости от атмосферного давления, наблюдались колебания температуры кипения в пределах от 154—155° до 158—159°.
Плотность:
1,514 (13°C, г/см3)
Давление паров (в мм.рт.ст.):
15 (58°C)
Источники информации:
- "Справочник химика" т.2, Л.-М.: Химия, 1964 стр. 1024-1025
выберите первую букву в названии статьи:
1-9
А Б В Г Д Е Ж З И К Л М Н О П Р С Т У Ф Х Ц Ч Ш Щ Э Ю Я
|


 7. Отделитель, показанный на рисунке, является видоизменением этого прибора, применяемого для определения содержания воды по методу Дина и Старка. Размеры отделителя можно изменять в зависимости от индивидуальных целей, поскольку этот вопрос касается главным образом удобства. Отделитель можно применять без внутренней воронки, но при ее наличии (К. Кельш, частное сообщение) конденсат разделяется на два слоя быстро и полностью, причем жидкость, стекающая из холодильника, не вызывает перемешивания обеих фаз в отделителе. Ножка воронки должна быть такой длины, чтобы верхний край воронки находился выше бокового отвода отделителя. Трубку отделителя можно градуировать, однако это не обязательно.
7. Отделитель, показанный на рисунке, является видоизменением этого прибора, применяемого для определения содержания воды по методу Дина и Старка. Размеры отделителя можно изменять в зависимости от индивидуальных целей, поскольку этот вопрос касается главным образом удобства. Отделитель можно применять без внутренней воронки, но при ее наличии (К. Кельш, частное сообщение) конденсат разделяется на два слоя быстро и полностью, причем жидкость, стекающая из холодильника, не вызывает перемешивания обеих фаз в отделителе. Ножка воронки должна быть такой длины, чтобы верхний край воронки находился выше бокового отвода отделителя. Трубку отделителя можно градуировать, однако это не обязательно.